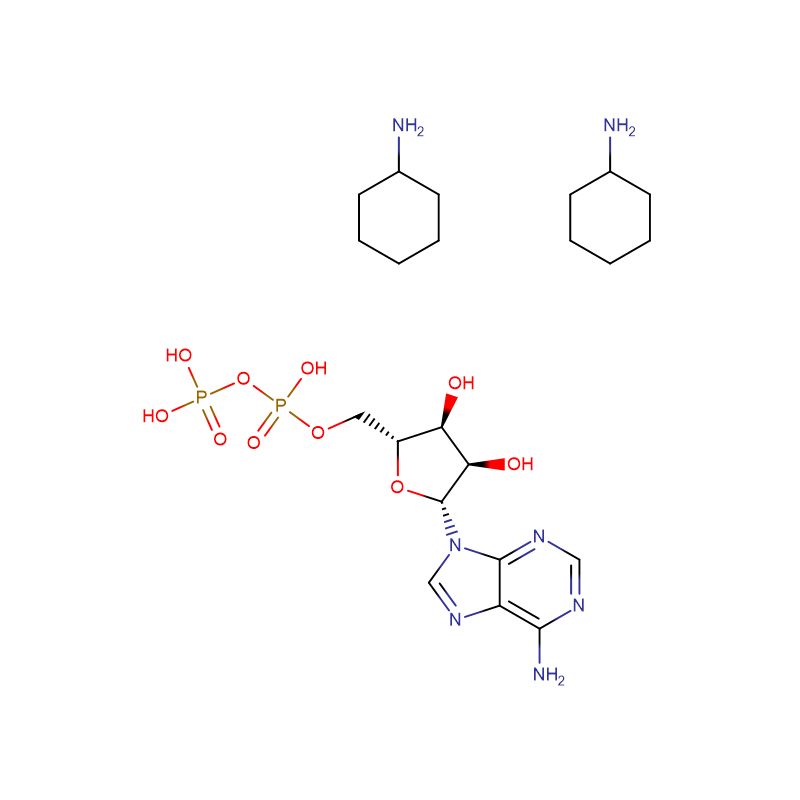
adenosine 5′-diphosphate di (monocyclohexylammoniu Cas: 102029-87-8 99% ผงสีขาว
| หมายเลขแคตตาล็อก | XD90159 |
| ชื่อผลิตภัณฑ์ | อะดีโนซีน 5'-ไดฟอสเฟต ได(โมโนไซโคลเฮกซิลแลมโมนิอู |
| CAS | 102029-87-8 |
| สูตรโมเลกุล | C10H15N5O10P2·2C6H13N |
| น้ำหนักโมเลกุล | 625.55 |
| รายละเอียดการจัดเก็บ | 2 ถึง 8 องศาเซลเซียส |
| รหัสภาษีที่สอดคล้องกัน |
คุณสมบัติของผลิตภัณฑ์
| รูปร่าง | ผงสีขาว |
| อาซาy | 99% |
1. เพื่อตรวจสอบว่า adenosine diphosphate (ADP) ที่ได้จาก adenosine อาจยับยั้งการรวมตัวของเกล็ดเลือดหรือไม่ โดยเฉพาะอย่างยิ่งเมื่อมี P2Y₁₂ antagonist โดยที่ผลของ ADP ที่ตัวรับ P2Y₁₂ จะถูกป้องกัน การรวมตัวของเกล็ดเลือดถูกวัดในการตอบสนองต่อ thrombin receptor activator เปปไทด์โดยการนับเกล็ดเลือดในพลาสมาที่อุดมด้วยเกล็ดเลือด (PRP) และเลือดครบส่วนต่อหน้า ADP และ cangrelor คู่อริ P2Y₁₂, prasugrel active metabolite และ ticagrelorเมื่อมี P2Y₁₂ antagonist การ preincubation ของ PRP ด้วย ADP ยับยั้งการรวมตัว;ผลกระทบนี้ถูกยกเลิกโดย adenosine deaminaseไม่มีการยับยั้งการรวมตัวเกิดขึ้นในเลือดครบส่วน ยกเว้นเมื่อเพิ่มไดไพริดาโมลเพื่อยับยั้งการดูดซึมอะดีโนซีนเข้าสู่เม็ดเลือดแดงผลกระทบของ ADP ใน PRP และเลือดครบส่วนถูกจำลองแบบโดยใช้อะดีโนซีน และเกี่ยวข้องโดยตรงกับการเปลี่ยนแปลงในแคมป์ (ประเมินโดยฟอสโฟรีเลชั่นที่กระตุ้นหลอดเลือด)ผลลัพธ์ทั้งหมดเหมือนกันโดยไม่คำนึงถึง P2Y₁₂ ant agonist ที่ใช้ ADP ยับยั้งการรวมตัวของเกล็ดเลือดเมื่อมี P2Y₁₂ antagonist ผ่านการเปลี่ยนเป็นอะดีโนซีนการยับยั้งเกิดขึ้นใน PRP แต่ไม่เกิดขึ้นในเลือดครบส่วน ยกเว้นเมื่อมีการยับยั้งการดูดซึมอะดีโนซีนไม่มีคู่อริ P2Y₁₂ ที่ศึกษาจำลองผลของไดไพริดาโมลในการทดลองที่ดำเนินการ
2.ADP ถือเป็นตัวกระตุ้นเกล็ดเลือดที่อ่อนแอเนื่องจากการตอบสนองการรวมตัวที่จำกัด มันชักนำในหลอดทดลองที่ความเข้มข้นทางสรีรวิทยาของ Ca(2+) นอกเซลล์ [(Ca(2+) )(o) ]การลด [Ca(2+) ](o) ที่ขัดแย้งกันจะช่วยเพิ่มการรวมตัวที่เกิดจาก ADP ซึ่งเป็นผลกระทบที่เกิดจากการผลิต thromboxane A(2) ที่ปรับปรุงแล้วการศึกษานี้ตรวจสอบบทบาทของเอคโตนิวคลีโอไทด์ใน [Ca(2+) ](o) -การพึ่งพาการกระตุ้นของเกล็ดเลือดการลด [Ca(2+) ](o) จากระดับมิลลิโมลาร์เป็นไมโครโมลาร์ที่แปลง ADP (10 ไมโครโมล/ลิตร) ทำให้เกิดการรวมตัวของเกล็ดเลือดจากชั่วคราวเป็นการตอบสนองที่ยั่งยืนทั้งในพลาสมาที่อุดมด้วยเกล็ดเลือดและสารแขวนลอยที่ถูกชะล้างการปิดกั้นการผลิต thromboxane A(2) ด้วยแอสไพรินไม่มีผลกระทบต่อ [Ca(2+) ](o) -dependence นี้การป้องกันการสลายตัวของ ADP ยกเลิกความแตกต่างระหว่างระดับต่ำและทางสรีรวิทยา [Ca(2+) ](o) ส่งผลให้เกิดการรวมตัวที่แข็งแกร่งและยั่งยืนในทั้งสองสภาวะการวัด ADP นอกเซลล์เผยให้เห็นการย่อยสลายที่ลดลงทั้งในพลาสมาและ apyrase-containin g saline ที่ไมโครโมลาร์เมื่อเทียบกับมิลลิโมลาร์ [Ca(2+) ](o)ตามที่รายงานก่อนหน้านี้ การสร้าง thromboxane A(2) ได้รับการปรับปรุงที่ระดับต่ำ [Ca(2+) ](o) อย่างไรก็ตาม สิ่งนี้ไม่ขึ้นอยู่กับกิจกรรมของ ectonucleotidase(.) cangrelor คู่อริตัวรับ P2Y และ MRS2179 แสดงให้เห็นถึงความจำเป็นของตัวรับ P2Y(12) สำหรับการรวมที่เกิดขึ้นจาก ADP ที่ยั่งยืน โดยมีบทบาทเล็กน้อยสำหรับ P2Y(1)โดยสรุป กิจกรรมของเอนไซม์เอคโตนิวคลีโอทิเดสที่ขึ้นกับ Ca(2+) เป็นปัจจัยสำคัญที่กำหนดขอบเขตของการรวมตัวของเกล็ดเลือดกับ ADP และต้องมีการควบคุมในการศึกษาการกระตุ้นตัวรับ P2Y